اقتربت زراعة “كلى الخنازير” في البشر من النجاح أكثر مما نتصور
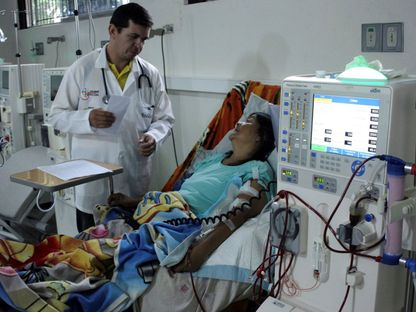
خرائط تفصيلية للتفاعل المناعي بين خلايا الإنسان وأعضاء الخنزير المزروعة
تمكن باحثون من رسم خرائط دقيقة لكيفية تفاعل الخلايا المناعية البشرية مع أنسجة الكلى المزروعة من خنازير معدلة وراثياً، وذلك باستخدام تقنيات تصوير جزيئي حديثة. تُعد هذه الدراسة خطوة مهمة نحو فهم عمليات الرفض المناعي وتحسين استراتيجيات العلاج بالتزامن مع التجارب السريرية الحالية لزرع كلى من خنازير إلى الإنسان.
تحديد الاستجابة المناعية ونافذة التدخل
- استخدم الباحثون تقنيات تصوير جزيئي مكاني متقدمة لتحديد أنماط استجابة الجهاز المناعي في مراحل مختلفة بعد الزرع.
- كشفت النتائج عن علامات جزيئية مبكرة للرفض، ظهرت بعد عشرة أيام، وبلغت ذروتها بعد 33 يوماً، مما يوفر نافذة زمنية مهمة للتدخل العلاجي المستهدف.
- تمت متابعة الاستجابة لمدة 61 يوماً، ما ساعد على تحديد «نافذة زمنية حرجة» يمكن خلالها التدخل لعلاج الرفض وتقليل احتماليته.
الآليات الرئيسية للرفض المناعي
تحدث عملية رفض الأعضاء المزروعة عبر آليتين رئيسيتين:
- الرفض بوساطة الخلايا التائية: حيث تتعرف الخلايا اللمفاوية التائية على المستضدات الغريبة وتهاجم الأنسجة المزروعة.
- الرفض بوساطة الأجسام المضادة: حيث تتشكل أجسام مضادة ضد مستضدات المتبرع وتلتصق بالأوعية الدموية، مما يسبب تلف العضو.
تطور التجارب السريرية وسعيها للسد الفجوة
تأتي هذه الأبحاث في وقت تتجه فيه التجارب السريرية نحو زرع كلى خنزير معدلة وراثياً للمرضى البشر، مع موافقة إدارة الغذاء والدواء على ذلك. تعتمد هذه التعديلات على عشرة تغييرات جينية، منها إضافة جينات بشرية وتعطيل أخرى، بهدف تقليل رفض الجهاز المناعي وتحسين التوافق.
نجاحات وتجارب عملية
- في مارس 2024، تلقى رجل يعاني من الفشل الكلوي أول زرعة كلية من خنزير معدلة وراثياً، ونجحت الكلية فورياً في أداء وظيفتها. على الرغم من وفاة المريض بعد شهرين، أوضح الأطباء أن الكلية كانت تؤدي وظيفتها بشكل جيد خلال الفترة، مما يبرز إمكانيات طويلة الأمد لهذا النهج.
- وفي نفس العام، تلقت امرأة أخرى كلية من خنزير معدل وراثياً، واحتفظت الكلية بوظيفتها لمدة 130 يوماً قبل أن يتم إزالتها بسبب رفض حاد.
التفاعل المناعي بين الإنسان والأعضاء المزروعة
توفر الدراسة الجديدة أدق خريطة للتفاعل المناعي بين الخلايا البشرية والأنسجة المزروعة من خنزير، حيث أظهر تحليل التعبير الجيني وسلوك الخلايا المناعية أن خلايا الماكروفاج والخلايا النخاعية كانت الأكثر انتشاراً، مع تأكيد دورها الرئيسي في عمليات الرفض المناعي.
عبر التدخلات العلاجية الموجهة، لوحظ انخفاض ملحوظ في مؤشرات الرفض، ما يفتح المجال لتطوير بروتوكولات علاجية أكثر دقة وفاعلية.
التحديات العالمية والنقص في الأعضاء
يظل نقص الأعضاء المتاحة للزراعة تحدياً كبيراً عالمياً، مع وجود أكثر من 100 ألف مريض ينتظرون عمليات زراعة في الولايات المتحدة وحدها، ومع نسبة عالية من مرضى الكلى المحتاجين إلى أعضاء جديدة.
- في عام 2024، تجاوزت عمليات زراعة الأعضاء 48 ألف عملية في الولايات المتحدة، مع زيادة طفيفة عن العام السابق، إلا أن الفجوة تتسع بشكل مستمر.
- الوفيات أثناء انتظار الأعضاء لا تزال تصل إلى حوالي 13 حالة يومياً في الولايات المتحدة، ويشهد العالم نقصاً كبيراً تزداد حدته يوماً بعد يوم.
آفاق تحسين العلاجات المناعية وتنويع الحلول
تشير الدراسات الحالية إلى أن تخطي عقبة الرفض المناعي أصبح أكثر إحتمالية، مع تطوير بروتوكولات علاجية مخصصة، وتصميم خلايا خنزير معدلة وراثياً بشكل أدق، لمواجهة تحديات الرفض قبل حدوثه.
على الرغم من أن دمج هذه التقنية في الممارسة الروتينية يتطلب سنوات من الأبحاث والاختبارات، فإن التقدم الحالي يضع الأساس لتحقيق زرع أعضاء من خنازير معدلة وراثياً كحل مستدام لمحاربة نقص الأعضاء عالمياً، وتحويلها إلى خيار علاجي مألوف في المستقبل القريب.