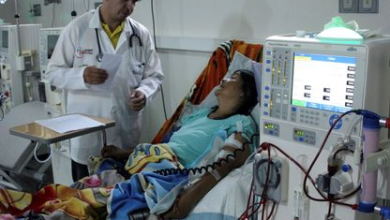
نجاح قريب من التحقيق: زرع “كلى الخنازير” في البشر
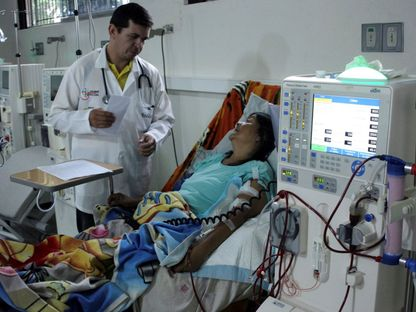
خارطة طريق جديدة لفهم التفاعل المناعي في عمليات زرع الأعضاء من الخنازير إلى البشر
شهدت الأبحاث العلمية تقدمًا ملحوظًا في مجال زراعة الأعضاء من الحيوانات المعدلة وراثيًا، وخاصة فيما يخص الكلى، حيث تمكن الباحثون من رسم خرائط مفصلة لكيفية تفاعل الخلايا المناعية البشرية مع أنسجة الكلى الخنزيرية المزروعة. ويستخدم العلماء تقنيات تصوير جزيئي مكاني حديثة لتحديد استجابة الجهاز المناعي، مما يفتح آفاقًا جديدة للتغلب على مشكلة رفض الأعضاء المزروعة.
التقدم في فهم رفض الأعضاء والتدخل العلاجي المبكر
- استخدم الباحثون أدوات متطورة لتحديد علامات جزيئية مبكرة تشير إلى الرفض المناعي، والتي ظهرت في اليوم العاشر بعد الزرع، وبلغت ذروتها في اليوم الليثالث والثلاثين.
- على مدار 61 يومًا من المراقبة، تم التعرف على “نافذة زمنية حرجة” يمكن التدخل خلالها لعلاج الرفض وزيادة فرص بقاء العضو المزروع.
آليات رفض الأعضاء المزروعة
تحدث حالة رفض الكلى أو أي عضو مزروع عندما يتعرف الجهاز المناعي على الأنسجة الجديدة على أنها غريبة، ويشن هجومًا مناعيًا بهدف تدميرها، وينطوي ذلك على آليتين رئيسيتين:
- الرفض بواسطة الخلايا التائية، حيث تتعرف الخلايا اللمفاوية على المستضدات الغريبة وتهاجم الأنسجة
- الرفض بواسطة الأجسام المضادة، التي تلتصق بالمستضدات وتسبب تلف الأوعية الدموية، مما يؤدي إلى تلف العضو
الخطوات المقبلة والتطبيقات السريرية
مع بدء التجارب السريرية لزرع الكلى المعدلة وراثيًا من الخنازير، والتي من المتوقع أن تبدأ في الولايات المتحدة خلال العام الحالي، تتجه الأبحاث نحو تحقيق توافق أكبر بين الأعضاء وخلايا الجهاز المناعي البشري. وتستخدم التعديلات الجينية لمعالجة الجينات التي قد تسبب رفضًا مناعيًا، مع التركيز على إضافة جينات بشرية وتعطيل جينات أخرى لتقليل الاستجابة المناعية.
قصص ناجحة وتحديات مستقبلية
في مارس 2024، كان أول من تلقى كلية خنزير معدلة وراثيًا هو رجل مصاب بالفشل الكلوي، وأظهرت الكلية وظيفة جيدة لفترة بعد الزرع، على الرغم من وفاته بعد حوالي شهرين؛ إلا أن النتائج أشارت إلى احتمالية تحقيق استدامة طويلة الأمد. وفي نفس العام، تلقت امرأة أخرى زراعة كلية، واستمرت لمدة 130 يومًا قبل أن تتعرض لرفض حاد.
التفاعل المناعي بين الإنسان والأعضاء المزروعة
تُقدم الدراسة الجديدة أدق تصور حتى الآن لطريقة تفاعل الجهاز المناعي مع الأعضاء المزروعة، وتُظهر أن خلايا الماكروفاج والخلايا النخاعية تلعب دورًا رئيسيًا في عمليات الرفض، مع إمكانية تعديل التدخلات العلاجية لتحقيق استجابات أكثر دقة وفعالية للحد من رفض الأعضاء.
التحديات العالمية في نقص الأعضاء
- يزداد الطلب على الأعضاء المزروعة بشكل كبير، بينما يظل العرض محدودًا. ففي الولايات المتحدة، ينتظر أكثر من 100 ألف شخص عمليات زرع، مع رغبة كبيرة في أعضائهم الكلى.
- رغم ارتفاع عدد عمليات الزرع، فإن العديد من المرضى يفقدون حياتهم أثناء الانتظار، مع مئات الحالات التي تتوفى سنويًا لعدم توفر الأعضاء المناسبة.
آفاق مستقبلية وتأثيراتها المحتملة
تشير الدراسات إلى أن تجاوز عقبة الرفض المناعي بات أقرب، وأن زراعة أعضاء الخنازير المعدلة وراثيًا يمكن أن تصبح خيارًا علاجيًا مستدامًا لمواجهة أزمة نقص الأعضاء. يعتقد الخبراء أن الزمن يقترب لزيادة دقة التقنيات وتحسين البروتوكولات العلاجية، مما يفتح الطريق لدمج هذه التقنية بشكل روتيني خلال السنوات القادمة.
وتتطلب الخطوات المستقبلية مواكبة طويلة من التجارب السريرية والتطوير التكنولوجي، وتعد هذه الدراسات بمثابة خطوة أساسية نحو تحويل زراعة أعضاء الخنازير إلى حل دائم يمكن أن يغير وجه الرعاية الصحية على مستوى العالم.