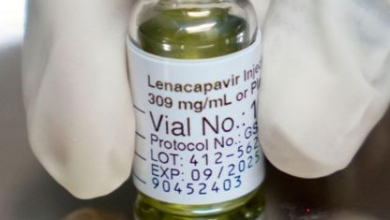نجاح زراعة “كلى الخنازير” في البشر يقترب أكثر مما نتصور
تقدم جديد في فهم المناعة وزراعة الأعضاء من الخنازير المعدلة وراثياً
لم يتمكن العلماء من رسم خرائط تفصيلية لتفاعل الخلايا المناعية البشرية مع أنسجة الكلى المزروعة من الخنازير، حيث تم الاعتماد على تقنيات تصوير جزيئي متطورة لتحديد الاستجابة المناعية بدقة عالية. هذا العمل يمثل خطوة مهمة نحو التغلب على التحديات الكبرى المتعلقة برفض الأعضاء المزروعة من الخنازير، ويفتح آفاقاً جديدة لزراعة الأعضاء الممولة وراثياً.
رسم خرائط التفاعل المناعي وتحديد علامات الرفض المبكرة
- باستخدام تقنيات تصوير جزيئي مكاني، تمكن الباحثون من تحديد استجابات المناعة البشرية بدقة تامة.
- كشفت النتائج عن وجود علامات جزيئية مبكرة للتفاعل المناعي، خاصة مع تزايد الأجسام المضادة، التي ظهرت في اليوم العاشر بعد الزرع وبلغت ذروتها في اليوم الثالث والثلاثين.
- هذه البيانات توفر نافذة زمنية محددة للتدخلات العلاجية المبكرة، بهدف تثبيط نوبات الرفض وتحسين احتمالات بقاء العضو المزروع على المدى الطويل.
تاريخ التفاعل والمراقبة بعد الزرع
تابع الفريق الاستجابات المناعية لمدة 61 يوماً، مما مكنهم من تحديد “نافذة زمنية حرجة” يمكن التدخل خلالها بهدف تقليل مخاطر رفض العضو.
آليات رفض الأعضاء المزروعة
- الرفض بوساطة الخلايا التائية: تتعرف الخلايا اللمفاوية التائية على المستضدات الغريبة وتتسبب في تلف الأنسجة.
- الرفض بوساطة الأجسام المضادة: تتكون أجسام مضادة ضد مستضدات المتبرع، وتلتصق ببطانة الأوعية الدموية، مما يؤدي إلى تلف العضو.
التجارب السريرية المستقبلية والآفاق
بدأت تجارب زراعة الكلى من الخنازير المعدلة وراثياً في البشر، حيث تم تعديل الأعضاء بشكل جيني يهدف إلى تقليل خطر الرفض. ومن بين هذه التعديلات إضافة جينات بشرية وتعطيل جينات أخرى تساعد في تقليل مقاومة الجسم للعضو المزروع.
في مارس 2024، كانت أول عملية زرع ناجحة لرجل يعاني من الفشل الكلوي، رغم وفاة المريض بعد شهرين، إلا أن الأطباء أكدوا على أن الكلية كانت تعمل بشكل جيد وليس سبب الوفاة، مما يعزز إمكانية استدامة الأعضاء المزروعة مستقبلاً.
وفي نوفمبر من نفس العام، تلقت امرأة أخرى كلية خنزير معدلة وراثياً، وظلت حياً لمدة 130 يوماً قبل أن يُزال العضو بسبب رفض مناعي حاد، مما يسلط الضوء على التحديات والتقدم في هذا المجال.
التفاعل المناعي بين الإنسان والأعضاء المزروعة من الخنازير
توفر الدراسة الحالية خريطة أكثر دقة لفهم تفاعل الجهاز المناعي مع الأنسجة المزروعة، حيث أظهرت أن خلايا الماكروفاج والخلايا النخاعية كانت من بين الأكثر انتشاراً، مما يدل على دورها الحاسم في عمليات الرفض المناعي.
كما أتاح استخدام الخوارزميات الحاسوبية تحليل أنماط التعبير الجيني وسلوك الخلايا، مما يسهل تطوير علاجات موجهة للتقليل من التفاعل المناعي الضار.
القضية العالمية لنقص الأعضاء وأهمية الحلول المبتكرة
- تواجه أنظمة الرعاية الصحية العالمية نقصاً حاداً في الأعضاء الصلبة اللازمة للزرع، حيث يتجاوز الطلب العرض بكثير.
- تُظهر الإحصائيات أن عدد عمليات الزرع سنوياً لا يزال أقل من الاحتياجات، مع وفاة العديد من المرضى أثناء انتظارهم.
- قد يكون زراعة الأعضاء من الخنازير المعدلة وراثياً حلاً واعداً لسد الفجوة وتحسين حياة المرضى بشكل كبير.
الآفاق والتحديات المستقبلية
على الرغم من التقدم، فإن تحويل زراعة أعضاء الخنازير إلى واقع عملي يتطلب سنوات من البحث والتجارب، بالإضافة إلى موافقات تنظيمية صارمة، لضمان السلامة والكفاءة لكل فئة من السكان.
يعمل الباحثون حالياً على تحسين التعديلات الوراثية، وتصميم بروتوكولات للكشف المبكر عن علامات الرفض، بهدف جعل زراعة الكلى من الخنازير خياراً علاجياً روتينياً خلال السنوات القادمة.
يأمل العلماء أن يؤدي هذا التطور إلى إحداث ثورة في مجال زراعة الأعضاء، مما يغير مستقبل الطب ويخفف من معاناة ملايين المرضى حول العالم.