صحة
نجاح زراعة كلى الخنازير في البشر يقترب أكثر مما نتصور
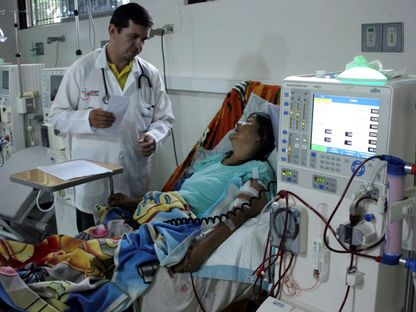
تقدم علمي في فهم التفاعل المناعي وتحسين زراعة الأعضاء من الخنازير المعدلة وراثياً
في ظل النقص العالمي الحاد في الأعضاء البشرية المتوفرة لعمليات الزراعة، تبرز تقنية زراعة أعضاء الخنازير المعدلة وراثياً كحل واعد يعكس تطوراً كبيراً في مجال الطب الحيوي. حيث تمكن باحثون من رسم خرائط تفصيلية لكيفية تفاعل الخلايا المناعية البشرية مع أنسجة الخنازير المزروعة، مما يعزز فرص نجاح هذه العمليات ويقلل من احتمالات رفض الأعضاء.
الاستجابة المناعية لزرع الكلى والخطوات الرئيسية للرفض
- الرفض بوساطة الخلايا التائية: حيث تتعرف الخلايا اللمفاوية التائية للمتلقي على المستضدات الغريبة على العضو المزروع وتعمل على تلف الأنسجة.
- الرفض بوساطة الأجسام المضادة: تتكون أجسام مضادة ضد مستضدات المتبرع، وتلتصق ببطانة الأوعية الدموية، مما يسبب تلف الجهاز العضوي.
التقدم في تجارب زراعة الأعضاء من الخنازير المعدلة وراثياً
- تم تعديل الكلى وراثياً عبر إضافة جينات بشرية وتعطيل جينات من الخنزير، بهدف تقليل مقاومة الجهاز المناعي البشري ورفض العضو.
- أول عملية زرع كلية خنزير معدلة وراثياً في مستشفى ماساتشوستس في مارس 2024، وأظهرت نجاحاً وظيفياً مبدئياً.
- تلتها حالة توانا لوني التي استمرت الكلية لديها لمدة 130 يوماً، مما يوضح إمكانية تحقيق استدامة أكبر في المستقبل.
الخرائط التفصيلية للتفاعل المناعي وتحليل خلايا الجهاز المناعي
استخدم الباحثون تقنيات تصوير جزيئي مكاني متطورة وخوارزميات معلوماتية حيوية لرسم خرائط دقيقة لانتشار وتفاعل الخلايا المناعية، مع تحديد خلايا الماكروفاج والخلايا النخاعية كبؤر رئيسية للرفض المناعي، مما يقدم فرصة للتدخل العلاجي المبكر وتقليل احتمالات رفض الأعضاء.
الآفاق والتحديات المستقبلية
- استمرار الأبحاث لتحسين التعديلات الوراثية للخنازير وتطوير بروتوكولات علاجية موجهة لخفض مستوى الرفض المناعي.
- التحدي الأكبر هو إثبات السلامة والفعالية عبر تجارب سريرية واسعة والموافقة عليها تنظيمياً.
- توقع أن يؤدي هذا التقدم إلى جعل زراعة الأعضاء من الخنازير خياراً علاجياً مستداماً خلال عقد من الزمن، مما يفتح آفاقاً واقعية لمعالجة أزمة نقص الأعضاء البشرية.