نجاح زراعة كلى الخنازير في البشر يقترب أكثر مما نتوقع
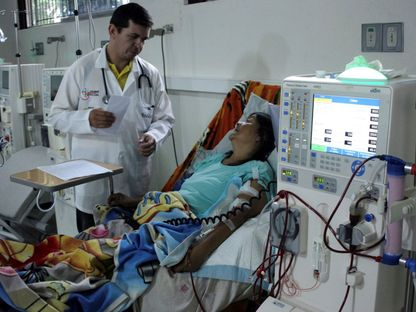
التقدم في فهم التفاعلات المناعية وتحسين زراعة الأعضاء من الخنازير المعدلة وراثياً
شهدت الأبحاث الحديثة تقدمًا ملحوظًا في تصور كيفية تفاعل خلايا الجهاز المناعي البشري مع الأنسجة المزروعة من الخنازير، خاصةً في سياق زرع الكلى. باستخدام تقنيات تصوير جزيئي مبتكرة، تمكن العلماء من رسم خرائط تفصيلية لهذه العمليات، مما يعزز فرص تطوير حلول طويلة الأمد لمرضى الفشل الكلوي.
إعادة رسم خريطة الاستجابة المناعية
- تم تحديد أنماط تعبير الجينات وسلوك الخلايا المناعية خلال فترة ما بعد الزرع، مع التركيز على خلايا الماكروفاج والخلايا النخاعية التي كانت الأكثر انتشاراً، مما يسلط الضوء على دورها الأساسي في عمليات الرفض المناعي.
- أظهرت الدراسة أن خلايا البلعمية الكبيرة، وهي خلايا دم بيضاء تملك قدرة على مهاجمة الكائنات الدقيقة وإزالة الخلايا الميتة، تلعب دوراً مركزياً في عمليات رفض الأعضاء، بالإضافة إلى الخلايا النخاعية التي تتنقل عبر الدم والجهاز اللمفاوي إلى مواقع تلف الأنسجة.
- استخدام الخوارزميات الحاسوبية ساعد على تمييز خلايا المناعة البشرية عن خلايا الأنسجة الخنزيرية، مما ساهم في رسم خريطة دقيقة لتسلل الجهاز المناعي إلى العضو المزروع.
تطوير استراتيجيات علاجية موجهة
- الإشارات إلى انخفاض ملحوظ في مؤشرات الرفض عند تطبيق تدخلات علاجية محددة، تشير إلى إمكانية تعطيل التفاعل المناعي الضار في المراحل المبكرة من العملية، مما يعزز فرص بقاء الأعضاء المزروعة على المدى الطويل.
- البحث يعزز فكرة أن التدخل المبكر عند ظهور علامات الاستجابة المناعية يمكن أن يحد من تطور الرفض، ويقرب من جعل زراعة الأعضاء من الخنازير خيارًا علاجياً مستدامًا.
الخطوات المستقبلية وتحديات النقص في الأعضاء
مع تزايد الطلب العالمي على الأعضاء ودراسة نتائج أولية لتجارب زرع كلى من الخنازير، بات من الواضح أن تقنيات التعديل الوراثي المتقدمة والرقابة الصارمة على سلامة الأعضاء هي مكونات أساسية لتوسيع هذا النهج.
التعديل الوراثي وزراعة الخنازير المعدلة
- تمت مراجعة عمليات زرع ناجحة، حيث تلقى المرضى كلى معدلة وراثياً مع استجابة فورية ووظائف مستقرة، رغم وفاة بعض المرضى لاحقاً لأسباب غير مرتبطة مباشرة بالرفض المناعي.
- التعديلات تشمل إضافة جينات بشرية وتعطيل أخرى من شأنها تقليل احتمالية رفض الأعضاء وتحسين مدى توافقها مع الجسم البشري، مما يتوقع أن يفتح آفاقًا جديدة أمام علاج أمراض الكلى.
التحدي العالمي لنقص الأعضاء
الضغط المتزايد على خدمات الزراعة يدفع نحو الاعتماد على الأعضاء المعدلة وراثياً كمصدر واعد لتعويض فجوة العرض والطلب، إذ أن حالات الانتظار في تزايد مستمر، مع معدلات وفاة مرتفعة أثناء الانتظار.
- على سبيل المثال، تنتظر مئات الآلاف حول العالم عمليات زرع، ومع أن الزيادة في عدد العمليات عام 2024 كانت مهمة، إلا أن الاحتياج يفوق بكثير القدرة على التلبية.
- تشير التقديرات إلى أن أقل من 10% من الحاجة العالمية للزراعة تُلبى حالياً، مما يبرز ضرورة تبني الحلول الحديثة والمبتكرة لتوفير الأعضاء.
آفاق تحسين العلاجات المناعية وتطوير بروتوكولات فعالة
تُظهر الدراسات أن فهم التفاعل على المستوى الجزيئي يساعد في تصميم تدخلات علاجية مخصصة، قد تقلل من مخاطر الرفض وتحسن نجاح عملية الزرع. رغم أن تطبيق هذه الحلول على نطاق واسع يتطلب سنوات من البحث والتجارب، فإن التقدم الحالي يقربنا من جعل زراعة الأعضاء من الخنازير خيارًا طبيعيًا ومستدامًا.
يأمل العلماء أن يؤدي هذا التقدم إلى تعزيز الإمكانيات العلاجية وتحويل مستقبل زراعة الأعضاء، مما يسهم في إنقاذ حياة مئات الآلاف حول العالم.




