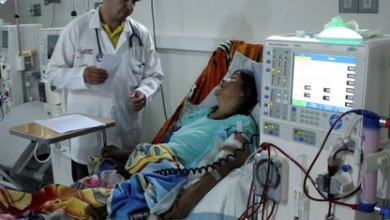
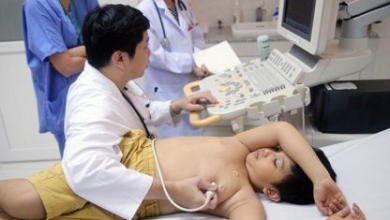
نجاح زراعة “كلى الخنازير” في البشر يقترب أكثر مما نتصور
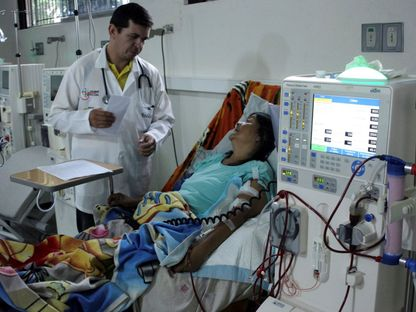
خرائط مفصلة للتفاعل المناعي بين خلايا الإنسان وأعضاء الخنزير المزروعة
تمكن فريق من الباحثين من إعداد خرائط دقيقة توضح كيف تتفاعل الخلايا المناعية البشرية مع أنسجة كلى الخنازير المعدلة وراثياً، وذلك باستخدام تقنيات تصوير جزيئي مكاني متطورة. يسعى هذا العمل إلى التغلب على أحد أكبر التحديات في زراعة الأعضاء الحيوانية، وهو رفض الجهاز المناعي.
التقدم في فهم عملية الرفض المناعي
- حدد الباحثون الاستجابة المناعية المبكرة لعمليات زرع الكلى من الخنازير إلى البشر، حيث ظهرت علامات مبكرة للرفض في اليوم العاشر بعد الزرع، وتضاعفت في اليوم الثالث والثلاثين.
- تُتيح النتائج تحديد نافذة زمنية حاسمة يمكن فيها التدخل العلاجي لتثبيط الرفض وزيادة فرص بقاء العضو المزروع.
- تابع الفريق الاستجابات المناعية لمدة 61 يوماً، مما أتاح تحديد فترة علاجية فعالة للحد من رفض العضو.
آليات الرفض المناعي
ويتضمن الرفض المناعي عمليات آلية رئيسية، منها:
- الرفض بواسطة الخلايا التائية: حيث تتعرف الخلايا اللمفاوية التائية على المستضدات الغريبة الموجودة على خلايا العضو المزروع، وتؤدي إلى تلف الأنسجة.
- الرفض بواسطة الأجسام المضادة: تتكون أجسام مضادة ضد مستضدات المتبرع، مما يسبب تلف الأوعية الدموية في العضو المزروع.
التفاعل المناعي وتقنيات العلاج
تُعد الدراسة مثالاً على التقدم في فهم كيف يتسلل الجهاز المناعي إلى العضو المزروع، وأظهرت الأدلة أن خلايا الماكروفاج والخلايا النخاعية كانت الأكثر انتشاراً، مما يؤكد دورها الكبير في عمليات الرفض. وأظهرت التدخلات العلاجية ملاحظة انخفاض ملحوظ في مؤشرات الرفض، موضحة إمكانية تعطيل التفاعل المناعي الضار.
تحديات نقص الأعضاء وزراعة الخنازير المعدلة وراثياً
يظل النقص العالمي الحاد في الأعضاء المزروعة يمثل مشكلة كبيرة، مع ارتفاع عدد المرضى الذين ينتظرون عمليات الزرع واختلاف توفياتهم أثناء الانتظار. على سبيل المثال، تنتظر أكثر من 100 ألف شخص في الولايات المتحدة، ويُركز معظمهم على زرع الكلى.
وفي عام 2024، تجاوزت عمليات زراعة الأعضاء 48 ألف عملية، منها حوالي 27 ألف عملية زرع كلى، مع زيادة طفيفة عن العام السابق، إلا أن الحاجة لا تزال تتجاوز العرض بشكل كبير، مما يترك العديد من المرضى في قوائم الانتظار ويفرض تكاليف بشرية واقتصادية عالية.
التطور في زراعة الأعضاء من الخنازير المعدلة وراثياً
- تمت الموافقة على إجراء تجارب سريرية لاستخدام كلى خنزير معدلة وراثياً، بعد أن نجحت في الحفاظ على وظيفة طويلة الأمد في بعض الحالات.
- تم تعديل الخنازير بعشرة تغييرات جينية، بما يشمل إضافة جينات بشرية وتعطيل جينات خنزيرية تقلل من رفض الأعضاء.
- يهدف هذا التعديل إلى تحسين التوافق بين الأعضاء البلهي والجهاز المناعي البشري، وتقليل احتمالية الرفض.
حالة زرع كلية خنزير معدلة وراثياً
في مارس 2024، تلقى رجل يبلغ من العمر 62 عاماً زرع كلية خنزير معدلة وراثياً بنجاح، مع استمرار أداء الكلية بشكل جيد، رغم وفاته بعد شهرين، إذ أكد الأطباء أن الوفاة لم تكن ناتجة عن رفض الأعضاء. وفي نوفمبر من العام ذاته، تلقت امرأة أخرى كلية من الخنزير، ورافقت وظيفة مستدامة لمدة 130 يوماً قبل أن يقرر الأطباء إزالتها بسبب رفض حاد.
التفاعل المناعي بين الإنسان والأعضاء المزروعة
توفر الدراسة الجديدة أول خريطة مفصلة للتفاعل المناعي بين الإنسان وعضو من الخنزير، بحيث يمكن تحديد أنماط تعبير الجينات وسلوك الخلايا المناعية، مما يعزز تطوير علاجات أكثر تخصصاً للحد من الرفض.
اعتمد الباحثون على خوارزميات معلوماتية حيوية لتمييز خلايا المناعة عن خلايا الأنسجة الخنزيرية، مع التركيز على الخلايا البلعمية الكبيرة والخلايا النخاعية، التي تبين أنها الأهم في عمليات الرفض المناعي.
الوظائف الرئيسية للخلايا البلعمية والخلايا النخاعية
- الخلايا البلعمية الكبيرة: خلويا الدم البيضاء المهمة التي تهاجم الملوثات والخلايا الميتة، وتحفز باقي خلايا الجهاز المناعي.
- الخلايا النخاعية: تضم أنواعاً متعددة تلعب أدواراً في المناعة الوقائية والتصدي للعدوى، وتصل إلى مواقع تلف الأنسجة عبر الدم والجهاز اللمفاوي.
آفاق العلاج وتقنيات التداخل
أظهرت نتائج الدراسة أن التدخلات العلاجية الموجهة أدت إلى انخفاض ملحوظ في مؤشرات الرفض المناعي، مما يدعم إمكانية تطوير بروتوكولات علاجية مخصصة للحد من التفاعل الضار، وتحقيق استدامة الأعضاء المزروعة.
آثار النقص في الأعضاء والحلول المبتكرة
يتفق الخبراء على أن زراعة الأعضاء من الخنازير المعدلة وراثياً تمثل حلاً واعداً لسد فجوة نقص الأعضاء، خاصة مع استمرار ارتفاع الطلب على عمليات الزرع، وارتفاع معدلات الوفاة أثناء الانتظار.
في الولايات المتحدة، يتوفى حوالي 13 شخصاً يومياً أثناء انتظارهم لزرع الأعضاء، بينما تجاوز عدد عمليات الزرع في عام 2024 نُظر اليه، إلا أنه لا يرقى إلى مستوى الطلب المتزايد.
تصل التقديرات العالمية لعام 2023 إلى أكثر من 172 ألف عملية زرع، مع أن الحاجة تتجاوز بكثير العرض الحالي، مما يستدعي تطوير ابتكارات جديدة لزيادة توافر الأعضاء.
اتجاهات المستقبل ودور الأبحاث
- تبقى دراسات تحسين العلاجات المناعية وتقنيات التعديل الوراثي للخنازير ذات أهمية كبرى لتحقيق عملية زراعة ناجحة ومستدامة على نطاق واسع.
- ويأمل العلماء أن يؤدي التقدم في فهم التفاعل الجزيئي إلى تطوير بروتوكولات علاجية مبكرة وفعالة، وإطلاق تطبيقات روتينية لزرع الأعضاء من الخنازير في المستقبل القريب.
يقول الخبراء إن الاعتماد الروتيني لهذا الحل يتطلب سنوات من التجارب والاختبارات، مع التأكيد على أهمية الموافقات التنظيمية والتأكيد على السلامة، بينما تظل الأبحاث في تطور مستمر نحو جعل زراعة الأعضاء من الخنازير خياراً علاجياً شبه قياسي خلال العقد القادم.