نجاح زراعة كلى الخنازير في البشر يقترب أكثر مما نتصور
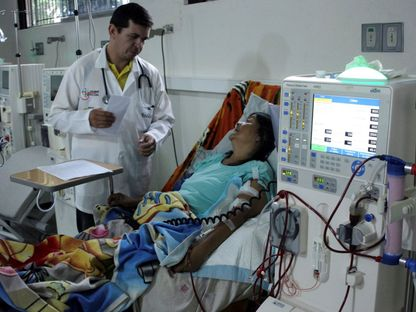
تقدم علمي في فهم تفاعل الخلايا المناعية مع أنسجة الخنازير المزروعة
تمكن فريق من الباحثين من رسم خرائط تفصيلية لآليات تفاعل الخلايا المناعية البشرية مع أنسجة كلى الخنازير المزروعة، باستخدام تقنيات تصوير جزيئي متطورة. وهدفت الدراسة إلى تحديد استجابة الجهاز المناعي للعضو المزروع في جسم الإنسان، بهدف التغلب على تحدي رفض الجهاز المناعي وزيادة فرص نجاح زراعة الأعضاء من الخنازير المعدلة وراثياً.
التقنيات والاكتشافات الرئيسية
- استخدام تقنيات تصوير جزيئي مكاني لتحديد استجابة الخلايا المناعية.
- رسم خرائط دقيقة لآليات التفاعل بين خلايا المناعة البشرية وأنسجة الكلى المزروعة.
- تحديد علامات جزيئية مبكرة للرفض من خلال الأجسام المضادة، والتي تظهر في اليوم العاشر بعد الزرع وتبلغ ذروتها في اليوم الثالث والثلاثين.
- مراقبة الاستجابات المناعية لمدة 61 يوماً لتحديد نافذة زمنية حرجة يمكن التدخل خلالها علاجياً لتثبيط الرفض وتحسين نجاح العضو المزروع.
الآليات الأساسية لرفض الأعضاء المزروعة
يحدث رفض الأعضاء المزروعة عندما يتعرف الجهاز المناعي للمريض على العضو باعتباره غريباً، ما يؤدي إلى هجوم مناعي يستهدف تدميره. وتنقسم آليات الرفض إلى:
- الرفض بواسطة الخلايا التائية، التي تتعرف على المستضدات الغريبة وتهاجم الأنسجة المزروعة.
- الرفض بواسطة الأجسام المضادة، التي تتكون ضد مستضدات المتبرع وتؤدي إلى تلف الأوعية الدموية للعضو المزروع.
التقدم في تجارب زرع الأعضاء من الخنازير
تستعد التجارب السريرية لزرع كلى من الخنازير المعدلة وراثياً في البشر، حيث وافقت إدارة الغذاء والدواء على إجراء هذه التجارب، باستخدام خنازير معدلة بعشرة تعديلات جينية لتعزيز التوافق مع الجهاز المناعي البشري وتقليل خطر الرفض.
حالات زرع ناجحة ومهمة
- في مارس 2024، تلقى رجل يبلغ من العمر 62 عاماً، يعاني من الفشل الكلوي، كلية خنزير معدلة وراثياً، واحتفظت الكلية بوظائفها لأكثر من شهرين قبل وفاة المريض، مع إشارات على إمكانية دوام وظيفة الكلية في المستقبل.
- وفي نوفمبر من نفس العام، تلقت امرأة أخرى من ألاباما كلية خنزير معدلة وراثياً، وظلت تعمل لمدة 130 يوماً قبل أن يتم إزالتها بسبب رفض حاد.
تفاعل الجهاز المناعي مع الأعضاء المزروعة
توفر الدراسة خريطة دقيقة لآليات التفاعل المناعي، حيث تبين أن الخلايا البلعمية الكبيرة، مثل الماكروفاج، والخلايا النخاعية، كانت الأكثر انتشاراً في جميع مراحل التفاعل، مما يؤكد دورها الرئيسي في عمليات رفض الأعضاء. وأظهرت التدخلات العلاجية الموجهة انخفاضاً ملحوظاً في مؤشرات الرفض، مما يفتح المجال لتطوير بروتوكولات أكثر دقة وفعالية لعلاج هذه الحالة.
الآفاق المستقبلية وتحديات النقص العالمي في الأعضاء
ماتزال أزمة نقص الأعضاء البشرية تمثل تحدياً كبيراً، حيث يحرم هذا النقص الآلاف من المرضى حول العالم من فرصة العلاج. على سبيل المثال، ينتظر أكثر من 100 ألف شخص في الولايات المتحدة فقط لزراعة أعضاء، مع وجود 86% منهم في حاجة ماسة لكلى جديدة. وعلى الرغم من زيادة عمليات الزرع بنسبة طفيفة، فإن الفجوة لا تزال كبيرة، ويتوفى يومياً العديد من المرضى بينما يظل العديد على قوائم الانتظار.
وتعد زراعة الأعضاء من الخنازير المعدلة وراثياً حلاً واعداً لسد هذه الفجوة، مع العلم أن تطوير هذا الخيار يتطلب سنوات من الأبحاث والتجارب، وضمان السلامة والفعالية، والحصول على الموافقات التنظيمية الضرورية. ويأمل الباحثون أن تساهم التعديلات الجينية والتحسينات المناعية المستمرة في جعل هذه التقنية خياراً روتينياً قريباً، مما يسهم في تغيير مستقبل زراعة الأعضاء على مستوى العالم.