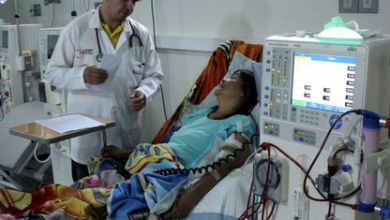
نجاح زراعة “كلى الخنازير” في البشر يقترب أكثر مما نتصور

خريطة التفاعلات المناعية في زرع الأعضاء من الخنازير إلى البشر
تمكن فريق من الباحثين من رسم خريطة تفصيلية لآليات تفاعل خلايا الجهاز المناعي البشرية مع أنسجة الكلى المزروعة من الخنازير، وذلك باستخدام تقنيات تصوير جزيئي متقدمة. تمثل هذه الدراسة خطوة مهمة نحو فهم كيفية التعامل مع التحدي الأكبر في زراعة الأعضاء من الخنزير، وهو رفض الجهاز المناعي، مما يمهد الطريق لتطوير طرق علاجية أكثر فاعلية وتقنيات زرع مستدامة.
التقنيات ودراسة الاستجابة المناعية
- استخدام تقنيات تصوير جزيئي مكانية عالية الدقة لتحديد مدى استجابة الخلايا المناعية، خاصة مكونات الخلايا البلعمية والخلايا النخاعية.
- تحليل أنماط تعبير الجينات لسلوك الخلايا المناعية وتحديد النمط الزمني للتفاعلات المناعية بعد الزرع.
- استنتاج أن الخلايا البلعمية الكبيرة والخلايا النخاعية كانت الأكثر انتشارًا أثناء عمليات الرفض، مما يشدد على دورها الأساسي في العملية المناعية.
الآليات الرئيسية للرفض المناعي
- الرفض بوساطة الخلايا التائية: تتعرف الخلايا اللمفاوية التائية على المستضدات الغريبة، وتهاجم الأنسجة المزروعة.
- الرفض بوساطة الأجسام المضادة: تتكون أجسام مضادة ضد مستضدات العضو، وتلتصق على الأوعية الدموية، مما يؤدي إلى تلف العضو وتحفيز استجابة مناعية شديدة.
توقيت الاستجابة والنافذة العلاجية الحساسة
تمت مراقبة الاستجابات المناعية لمدة تزيد عن شهرين بعد الزرع، وكُشفت نافذة زمنية حاسمة يُعتقد أنها مثالية للتدخل العلاجي بهدف تثبيط رفض العضو، مما يعزز احتمالات استدامة الأعضاء المزروعة ومحدودية الحاجة إلى علاجات مناعية طويلة الأمد.
مستقبل زرع الأعضاء من الخنزير للبشر
- تشهد عمليات التجارب السريرية للتبرع كلية معدلة وراثياً من الخنازير انتشارًا، مع توقعات بتوسيعها خلال السنوات القادمة.
- اعتمدت إدارة الغذاء والدواء على هذه الأبحاث لمنح الموافقات اللازمة، مما يفتح آفاقًا جديدة لعلاج مرضى الفشل الكلوي من خلال الأعضاء المعدلة وراثياً.
- تتضمن التعديلات الجينية إدخال جينات بشرية وتعطيل جينات من الخنزير تقلل من احتمالية رفض الجهاز المناعي، مما يعزز بعد التوافق وتحسين فرص البقاء الدائم للعضو المزروع.
نماذج حية وتجارب واقعية
على سبيل المثال، في مارس 2024، أجرى فريق طبي عملية زرع كلية خنزير معدلة وراثياً لأول مرة في مريض بشري، وأظهرت الكلية استجابة جيدة ووظائف مستقرة لعدة أسابيع قبل أن يخفق المريض لأسباب غير مرتبطة برفض الكلية بشكل حاد. كما تلقت امرأة أخرى في نفس العام كلية خنزير معدلة وراثياً واستمرت في العمل لمدة 130 يومًا قبل أن يطرأ رفض حاد، مما يسلط الضوء على التحديات والتقدم المستمر في المجال.
التحديات الحالية وأفاق المستقبل
- يظل النقص العالمي في الأعضاء العضويّة تحدياً كبيراً يهدد حياة العديد من المرضى، مع تزايد الطلب وتقليل العرض.
- تواصل الدراسات في تحسين البروتوكولات العلاجية، وتعزيز التعديلات الجينية للخنازير، وتطوير أدوات للكشف المبكر عن الرفض، بهدف جعل زرع الأعضاء من الخنازير خياراً آمنًا وفعالاً على المدى الطويل.
- يشدد الخبراء على أن عملية الاعتماد على الزراعة من الخنازير ستتطلب سنوات من التجارب السريرية والإثباتات العلمية، لكن الأفق يبدو أكثر إشراقاً بفضل هذه الأبحاث المتقدمة.
وفي المحصلة، تُعد هذه الدراسة خطوة مهمة نحو تحقيق هدف أنهاء أزمة نقص الأعضاء، مع تهيئة الطريق لإحلال الأعضاء المعدلة وراثياً كحل طبي مستدام، وواعد، يعيد الأمل لآلاف المرضى حول العالم.