إقتراب نجاح زراعة كلى الخنازير في البشر أكثر مما نتوقع
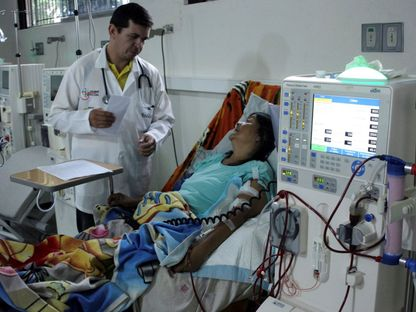
رسم خرائط متقدمة لتفاعل الخلايا المناعية مع أنسجة الكلى الخنزيرية
تمكن فريق من الباحثين من إنشاء خرائط تفصيلية لكيفية تفاعل الخلايا المناعية البشرية مع أنسجة الكلى المزرعة في الخنازير، باستخدام تقنيات تصوير جزيئي مكاني حديثة ومتطورة. ويأتي هذا الإنجاز كخطوة مهمة نحو فهم عملية رفض الأعضاء المزروعة وتطوير استراتيجيات علاجية أكثر دقة وفعالية.
تحديد الاستجابة المناعية لزرع الكلى الخنزيرية بالبشر
- استخدام تقنيات تصوير جزيئي مكاني لتحديد علامات جزيئية مبكرة لعملية الرفض، والتي ظهرت بشكل واضح منذ اليوم العاشر من الزرع، وبلغت ذروتها في اليوم الثلاثين والثالث والثلاثين بعد الزرع.
- تقديم نافذة زمنية حاسمة للتدخل العلاجي، حيث استمرت الدراسة لمدة 61 يوماً بعد الزرع، بهدف تحسين فرص بقاء العضو المزروع وتثبيط عمليات الرفض.
آليات رفض الأعضاء المزروعة
يحدث رفض الكلى أو أي عضو مزروع نتيجة تعرف الجهاز المناعي على العضو كغريب، مما يؤدي إلى استجابات مناعية متنوعة تشمل:
- الرفض بواسطة الخلايا التائية: حيث تتعرف الخلايا اللمفاوية التائية على المستضدات الغريبة وتهاجم الأنسجة.
- الرفض بواسطة الأجسام المضادة: تتكون أجسام مضادة ضد مستضدات المتبرع وتسبب تلف الأوعية الدموية للعضو المزروع.
تقدم الأبحاث والتجارب السريرية
شهد عام 2024 إطلاق أولى التجارب السريرية لزرع كلى خنزير معدلة وراثياً في بشر، حيث أُجريت العمليات بنجاح نسبي في مراحلها الأولى، مبرزة إمكانية الاستخدام المستقبلي لهذا النهج. وتعد الكلى المعدلة، التي خضعت لعشرة تعديلات جينية، أكثر توافقاً مع الجهاز المناعي البشري وتقلل من احتمالية الرفض.
تفاعلات المناعة بين الإنسان والخلايا المزروعة
توفر الدراسة الحالية أدق خريطة للتفاعل المناعي بين الإنسان وأنسجة الخنزير المجمعة، حيث أظهرت النتائج أن خلايا البلعمية الكبيرة (الماكروفاج) والخلايا النخاعية كانت الأكثر انتشاراً، مما يعكس دورها الرئيسي في عمليات الرفض المناعي.
وقد أظهرت التدخلات العلاجية الموجهة انخفاضًا ملحوظًا في مؤشرات الرفض، الأمر الذي يفتح آفاق تطوير بروتوكولات علاجية أكثر استهدافًا وفاعلية.
التحديات والحاجة إلى حلول مبتكرة
- تتزايد الحاجة إلى الأعضاء المزروعة عالميًا، حيث يعاني آلاف المرضى من نقص حاد في الأعضاء، مع وجود قائمة انتظار طويلة تتجاوز الطلب بشكل كبير.
- فمثلاً، في الولايات المتحدة، يوجد أكثر من 100 ألف مريض على قوائم الانتظار، وتوفي مئات منهم أثناء انتظارهم، ويُعد مرض الكلى الأكثر شيوعًا بين المحتاجين.
ورغم زيادة عدد عمليات الزرع، فإن الفجوة بين العرض والطلب لا تزال قائمة، مما يدعو إلى تعزيز البحث والاستثمار في استراتيجيات زراعة الأعضاء من الخنازير المعدلة وراثياً كحل مستقبلي وواعد.
آفاق مستقبلية وتطوير العلاجات المناعية
- توضح الدراسة أن فهم التفاعلات الجزيئية يُمكّن من تصميم تدخلات وقائية قبل تطور الرفض، مما يمهد الطريق لزرعات أكثر أمانًا ونجاحًا.
- على المدى الطويل، يطمح الباحثون إلى تحسين التعديلات الوراثية للخنازير وتطوير بروتوكولات إنذار مبكر للكشف عن علامات الرفض والتدخل العلاجي المبكر.
ويأمل الخبراء أن تؤدي هذه الأبحاث إلى تحويل زراعة أعضاء الخنزير إلى خيار علاجي روتيني خلال العقد القادم، مما يساهم في حل أزمة نقص الأعضاء وتحسين حياة الملايين حول العالم.




