نجاح زراعة كلى الخنازير في البشر يقترب أكثر من توقعاتنا
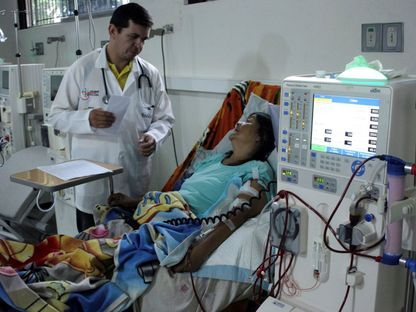
رسم خرائط تفاعل الخلايا المناعية في أنسجة الكلى من الخنازير وتطبيقاتها المستقبلية
أظهرت دراسات حديثة تقدمًا ملحوظًا في فهم التفاعل بين الجهاز المناعي البشري وأعضاء الخنازير المعدلة وراثيًا، مما يعزز آفاق تطوير زراعة أعضاء من الحيوانات بدلاً من الاعتماد الكلي على الأعضاء البشرية المحدودة.
تحديد استجابة الجهاز المناعي بعد زرع الكلى من الخنازير
- باستخدام تقنيات تصوير جزيئي متطورة، تمكن الباحثون من رسم خريطة مفصلة لكيفية استجابة الخلايا المناعية البشرية للأنسجة المزروعة من الخنازير المعدلة وراثياً.
- كشفت النتائج عن علامات جزيئية مبكرة للرفض، ظهرت في اليوم العاشر بعد الزرع ووصلت إلى ذروتها في اليوم الثالث والثلاثين.
- هذا التحديد المبكر للعلامات يسمح بالتدخل العلاجي في نافذة زمنية حاسمة لتقليل احتمالية رفض العضو وزيادة فرص بقائه على المدى الطويل.
آليات رفض الأعضاء المزروعة وكيفية التعامل معها
تتعدد آليات رفض الأعضاء المزروعة، وأهمها:
- الرفض بواسطة الخلايا التائية: حيث تتعرف الخلايا الليمفاوية على المستضدات الغريبة وتهاجم الأنسجة المزروعة.
- الرفض بواسطة الأجسام المضادة: حيث تتشكل أجسام مضادة ضد مستضدات المتبرع وتؤدي إلى تلف العضو.
تطور تجارب زرع الكلى من الخنازير المعدلة وراثيًا
- تمت الموافقة على التجارب السريرية في الولايات المتحدة باستخدام كلى خنازير معدلة وراثيًا بعشرة تعديلات جينية، تشمل إضافة جينات بشرية وتعطيل جينات من الخنزير تقلل من احتمالية رفض الجهاز المناعي.
- وفي 16 مارس 2024، تلقى رجل يعاني من الفشل الكلوي أول زرعة ناجحة لكن لم تدم الوظيفة طويلًا، مما يسلط الضوء على إمكانية استمرار نجاح هذه التقنية.
- وفي نوفمبر من نفس العام، تلقت امرأة أخرى كلى خنزير معدلة وراثيًا، وأظهرت نتائج جيدة استمرت لمدة 130 يومًا قبل حدوث رفض حاد أدى إلى إزالتها.
التفاعل المناعي بين الإنسان والأعضاء المزروعة من الخنازير
توفر الدراسات الحالية خريطة دقيقة لتفاعل الخلايا المناعية، حيث تبين أن الخلايا البلعمية الكبيرة والخلايا النخاعية تلعب دورًا رئيسيًا في عمليات الرفض.
- كشف التحليل أن هذه الخلايا كانت الأكثر انتشارًا، مما يعزز فهمنا لكيفية استهدافها لتقليل الرفض.
- على إثر ذلك، أُجريت تدخلات علاجية أدت إلى تقليل مؤشرات الرفض، ما يشجع على تطوير علاجات موجهة وفعالة مستقبلًا.
تحديات نقص الأعضاء والحلول المستقبلية
- على الرغم من التقدم، لا تزال أزمة نقص الأعضاء تمثل تحديًا عالميًا، حيث ينتظر ملايين المرضى عمليات زرع حياة.
- في الولايات المتحدة وفرنسا، تتجاوز أعداد الوفيات المرتبطة بعدم وجود الأعضاء الكافية الآلاف سنويًا.
- وتشير التقديرات إلى أن أقل من 10% من الاحتياج العالمي مُحقق حاليًا، الأمر الذي يسلط الضوء على الحاجة الماسة إلى حلول مبتكرة.
آفاق تحسين العلاجات وتقنيات الزراعة من الخنازير
يعكف الباحثون حاليًا على تطوير بروتوكولات علاج مناعي مخصصة، وتحسين التعديلات الوراثية على الخنازير، بهدف جعل زراعة الأعضاء أكثر أمانًا وفاعلية.
يُرجح أن تستغرق هذه الجهود سنوات قبل أن تصبح الزراعة الروتينية، إلا أن النتائج الحالية تشير إلى أن زراعة الكلى من الخنازير أصبحت أقرب من أي وقت مضى إلى أن تصبح خيارًا علاجيًا مقبولاً.
من المتوقع أن يؤدي هذا التقدم إلى إحداث ثورة في مجال زراعة الأعضاء، مما يخفف من وطأة أزمة نقص الأعضاء ويعيد الأمل للعديد من المرضى حول العالم.




