نجاح زراعة كلى الخنازير في البشر يقترب أكثر مما نتصور
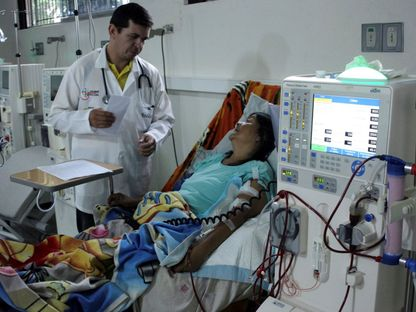
خرائط مفصلة لاستجابة الجهاز المناعي عند زراعة الأعضاء من الخنازير للبشر
تمكن فريق من الباحثين من رسم خرائط تفصيلية لكيفية تفاعل الخلايا المناعية البشرية مع أنسجة الكلى المزروعة من الخنازير، وذلك باستخدام تقنيات تصوير جزيئي متطورة. يأتي هذا الإنجاز في إطار الجهود المبذولة للتغلب على التحدي الأكبر في زراعة الأعضاء من الخنازير وهو رفض الجهاز المناعي للعضو المزروع، مما يفتح آفاقاً جديدة لعلاج مرضى الفشل العضوي.
التقدم في فهم التفاعل المناعي
- كشفت الدراسة عن علامات جزيئية مبكرة لرفض الأعضاء، التي تظهر في اليوم العاشر بعد الزراعة وتبلغ ذروتها في اليوم الثالث والثلاثين، مما يتيح فرصة التدخل العلاجية المبكر.
- استمرت تتبع استجابات الجهاز المناعي لمدة 61 يوماً، مما ساعد على تحديد “نافذة زمنية حرجة” يمكن خلالها تنفيذ علاجات لتثبيط الرفض وتحسين فرص بقاء العضو المزروع.
آليات رفض الأعضاء المزروعة
يحدث رفض الأعضاء المزروعة عندما يتعرف الجهاز المناعي للمريض على العضو كجسم غريب، حيث تتضمن الآليتان الرئيسيتان:
- الرفض بواسطة خلايا تائية: تتعرف الخلايا اللمفاوية التائية على المستضدات الغريبة وتتسلل إلى الأنسجة لتلفها.
- الرفض بواسطة الأجسام المضادة: تتكون أجسام مضادة ضد مستضدات المتبرع وتلتصق ببطانة الأوعية الدموية، مما يؤدي إلى تلف العضو وزيادة احتمالية رفضه.
تطوير الأعضاء المزروعة من الخنازير المعدلة وراثياً
تُعد عمليات الزرع من الخنازير المعدلة وراثياً، التي تتضمن إضافة جينات بشرية وتعطيل جينات من الخنزير، خطوة مهمة نحو تقليل رفض الأعضاء. ففي فبراير 2025، وافقت إدارة الغذاء والدواء الأمريكية على إجراء تجارب سريرية تشمل كلى خنازير معدلة، مما يمهد الطريق لاستخدامها كبديل مستدام.
أمثلة على حالات الزرع الناجحة والمؤشرات المستقبلية
- في مارس 2024، تلقى رجل يبلغ من العمر 62 عاماً، يعاني من الفشل الكلوي، أول زرعة كلية من خنزير معدل وراثياً، واستمرت الكلية تعمل بشكل جيد لمدة شهرين رغم وفاة المريض لاحقاً، دون أن تكون الكلية سبب الوفاة.
- وفي نوفمبر 2024، تلقّت امرأة من ألاباما، تبلغ من العمر 53 عاماً، كلية خنزير معدلة، وظلت تعمل لمدة 130 يوماً قبل أن يتم إزالتها بسبب رفض حاد.
التفاعل المناعي بين الإنسان والأعضاء المزروعة
توفر الدراسة أدق خريطة حتى الآن لهذا التفاعل، حيث يمكن تحديد أنماط تعبير الجينات وسلوك الخلايا المناعية. كشفت النتائج عن أن خلايا الماكروفاج والخلايا النخاعية كانت الأكثر انتشاراً، وتلعب دوراً رئيسياً في عمليات الرفض المناعي، مما يعزز من إمكانية تطوير علاجات موجهة لتثبيط التفاعل المناعي الضار في مراحله المبكرة.
التحديات والأفق المستقبلي
- يظل نقص الأعضاء البشرية أحد أكبر التحديات، مع استمرار الاعتماد على زراعة الأعضاء من الخنازير المعدلة وراثياً كمصدر محتمل لتلبية الطلب المتزايد.
- شهد عام 2024 زيادة طفيفة في عدد عمليات الزرع، إلا أن الفجوة بين العرض والطلب لا تزال واسعة، مع وفاة عشرات المرضى يومياً أثناء انتظارهم للأعضاء.
- يشدد الباحثون على أن فهم التفاعل المناعي على المستوى الجزيئي يفتح الباب لتطوير بروتوكولات علاجية أكثر دقة وفعالية، ومع الوقت، يُتوقع أن تُصبح زراعة الأعضاء من الخنازير خياراً علاجياً مستداماً.
ختام
يُعد هذا التقدم خطوة مهمة على طريق جعل زراعة الأعضاء من الخنازير المعدلة وراثياً خياراً فعالاً وآمناً، مع إمكانيات لتحسين حياة آلاف المرضى حول العالم. وتستمر الأبحاث في تعزيز فهمنا للآليات المناعية، لتقليل معدلات الرفض وتحقيق نجاحات أكبر في المستقبل القريب.