نجاح زراعة “كلى الخنازير” في البشر يقترب أكثر مما نعتقد
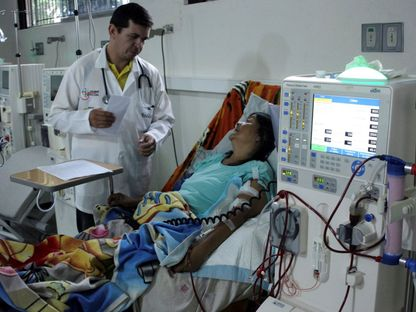
خرائط دقيقة لتفاعل الخلايا المناعية مع أنسجة الخنازير وتطورات زرع الأعضاء المعدلة وراثياً
تمكن باحثون من رسم خرائط تفصيلية لكيفية تفاعل الخلايا المناعية البشرية مع أنسجة كلى الخنازير المزروعة، باستخدام تقنيات تصوير جزيئي مكاني متطورة. يأتي هذا الإنجاز في إطار السعي للتغلب على التحدي الأكبر في زراعة الأعضاء من الخنازير، وهو رفض الجهاز المناعي للعضو المزروع، مما قد يفتح آفاقاً جديدة لعلاج نقص الأعضاء عالمياً.
التفاعل المناعي والكشف المبكر عن الرفض
- حددت الدراسة علامات جزيئية مبكرة لعملية الرفض بوساطة الأجسام المضادة، تظهر في اليوم العاشر بعد الزرع وتصل إلى ذروتها في اليوم الثالث والثلاثين.
- عبر تتبع استجابة المناعة لمدة 61 يوماً، تمكن الفريق من تحديد “نافذة زمنية حرجة” يمكن التدخل فيها علاجياً لمنع رفض العضو وتحسين فرص استمراره.
آليات رفض الأعضاء المزروعة
يحدث رفض الأعضاء المزروعة عندما يتعرف الجهاز المناعي على العضو كغرباء، فيشن هجوماً بهدف تدميره، ويقوم على آليتين رئيسيتين:
- الرفض بوساطة الخلايا اللمفاوية التائية: حيث تتعرف الخلايا التائية على المستضدات الغريبة وتهاجم الأنسجة.
- الرفض بوساطة الأجسام المضادة: حيث تتشكل أجسام مضادة ضد مستضدات المتبرع، مما يؤدي إلى تلف الأوعية الدموية وتدمير العضو.
تقدم في تجارب زراعة الأعضاء من الخنازير
- تم قبول إجراء تجارب سريرية لزرع كلى من خنازير معدلة وراثياً في متلقين بشريين، مع بداية التجارب في الولايات المتحدة هذا العام.
- تمت الموافقة على إجراء هذه التجارب من قبل إدارة الغذاء والدواء، باستخدام كلى معدلة جينياً بعشرة تعديلات، بما يشمل إضافة جينات بشرية وتعطيل أخرى لتقليل خطر الرفض المناعي.
حالات زرع ناجحة وتحديات مستقبلية
- في 16 مارس 2024، تلقى رجل يبلغ من العمر 62 عاماً، يعاني من الفشل الكلوي، أول زرعة كلية خنزير معدلة وراثياً في مستشفى ماساتشوستس، واستمرت الكلية بالوظيفة لمدة شهرين تقريباً دون أن تكون سبب الوفاة.
- وفي نوفمبر من نفس العام، تم زرع كلية من خنزير معدّل لامرأة أخرى، واستمرت لمدة 130 يوماً قبل أن تتعرض لرفض حاد.
تفاعل الجهاز المناعي وفوائد رسم الخرائط الجديدة
توفر الدراسة الجديدة أدق خريطة لتفاعل الجهاز المناعي مع الأعضاء المزروعة من الخنازير، حيث أظهرت النتائج أن خلايا الماكروفاج والخلايا النخاعية كانت الأكثر انتشاراً، مؤكدة دورها الرئيسي في عمليات الرفض. يمكن من خلال تحديد أنماط التعبير الجيني أن نطور علاجات موجهة تقلل من خطر الرفض، مما يعزز أمل توسيع استخدام زراعة الأعضاء من الخنازير.
التحديات العالمية في نقص الأعضاء وإمكانات الحلول المستقبلية
مما لا شك فيه أن النقص العالمي الحاد في الأعضاء المزروعة يمثل أزمة صحية وإنسانية كبرى، حيث يُنتظر آلاف المرضى في قوائم الانتظار سنوياً، بينما يموت العديد منهم قبل أن يحظوا بفرصة للعلاج، خاصةً مرضى الكلى.
- رغم زيادة عمليات الزرع في بعض الدول، إلا أنها لا تلبي الحاجة المتزايدة، ويبرز توسيع استخدام الأعضاء المعدلة وراثياً كحلاً واعداً لهذه الأزمة.
- مع تقدم الدراسات، يُتوقع أن يمر عاملاً تحسن تتضمن تعديل الإجراءات العلاجية وتطوير بروتوكولات للكشف المبكر عن علامات الرفض، بهدف جعل زراعة الأعضاء من الخنازير خياراً علاجياً أكثر اعتماداً على نطاق واسع.
ختام وتطلعات المستقبل
يشير الخبراء إلى أن فهم التفاعل المناعي على المستوى الجزيئي يقترب من تمهيد الطريق للزراعات الحيوية المستدامة، مع إمكانات لتحسين سلامة وفعالية هذه العمليات في مختلف الفئات السكانية، وتقليل الاعتمادية على الأعضاء البشرية المتاحة حالياً. ويعد هذا التقدم خطوة مهمة نحو جعل زراعة أعضاء الخنازير خياراً روتينياً خلال العقد القادم، ليحدث ثورة في مجال علاج الفشل العضوي على مستوى العالم.




