نجاح زراعة كلى خنازير في البشر يقترب أكثر مما كنا نتصور
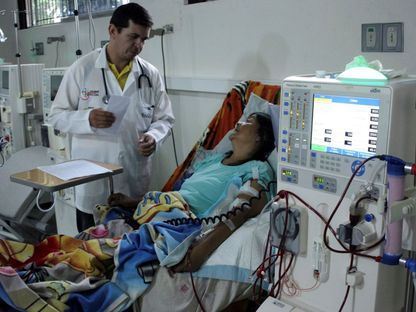
تطورات في فهم التفاعلات المناعية للزرع من الخنازير والبؤر ذات الصلة
شهدت أبحاث حديثة تقدمًا مهمًا في مجال زراعة الأعضاء من الخنازير المعدلة وراثيًا، حيث تمكن العلماء من رسم خرائط دقيقة لآليات تفاعل الجهاز المناعي البشري مع الأنسجة المزروعة. وهذه الدراسة تفتح الأفق أمام حلول فعالة لمشكلة نقص الأعضاء المزروعة على مستوى العالم.
رسم الخرائط للتفاعل المناعي وتحديد علامات الرفض المبكرة
- باستخدام تقنيات تصوير جزيئي متطورة، قام الباحثون بتحديد استجابة الجهاز المناعي للبشرات بعد زرع كلى من الخنازير المعدلة وراثيًا.
- تحدد الدراسة علامات جزيئية واضحة تظهر مبكرًا، حيث ظهرت أولى علامات الرفض بعد عشرة أيام من الزرع، وبلغت ذروتها عند اليوم الثالث والثلاثين.
- هذه النتائج تؤكد أن فترات التدخل العلاجي المبكر يمكن أن تقلل من احتمالية رفض الأعضاء المزروعة وتزيد من فرص بقائها على المدى الطويل.
الآليات الأساسية لرفض الأعضاء المزروعة
تحدث غالبية حالات رفض الأعضاء عبر آليتين رئيسيتين:
- الرفض باستخدام الخلايا التائية: حيث تتعرف الخلايا اللمفاوية على المستضدات الغريبة وتهاجمها، مما يسبب تلف الأنسجة.
- الرفض بواسطة الأجسام المضادة: حيث تتشكل أجسام مضادة ضد مستضدات المانح، وتصبح بطانة الأوعية الدموية معرضة لهجمات مناعية تؤدي إلى تلف العضو.
الأبحاث السريرية والتطبيقات المستقبلية
مع اقتراب التجارب السريرية لزرع كلى من الخنازير المعدلة وراثيًا إلى مرحلة التطبيق، تتطلع الأوساط العلمية إلى تحسين معدلات النجاح وتقليل احتمالات رفض الجهاز المناعي. وقد وافقت إدارة الغذاء والدواء على إجراء مثل هذه التجارب، باستخدام أعضاء معدلة جينيًا لتحقيق توافق أكبر مع الجسم البشري.
الزراعة من الخنازير المعدلة وراثيًا: إنجازات وأمثلة حية
- في مارس 2024، خضع رجل يعاني من الفشل الكلوي لزرع أول كلية من خنزير معدل وراثيًا، ونجحت الكلية في العمل بشكل جيد خلال الأشهر الأولى قبل أن تتوفى الحالة لأسباب غير مرتبطة بوظيفة الكلية.
- وفي نوفمبر من العام نفسه، تلقت امرأة أخرى في ولاية نيويورك كلية معدلة وراثيًا، وظلت تعمل لمدة 130 يومًا قبل أن تتوقف بسبب رفض مناعي حاد.
الفهم المتقدم للتفاعل المناعي بين الإنسان والأعضاء المزروعة
من خلال التحليل الشامل لأنماط التعبير الجيني وسلوك الخلايا المناعية، أتاح الباحثون رسم خارطة مفصلة لكيفية تسلل الجهاز المناعي إلى الأعضاء المزروعة. وتبين أن خلايا الماكروفاج والخلايا النخاعية تقع في مركز التفاعل، حيث تلعب دورًا رئيسيًا في عمليات رفض الأعضاء.
وقد أظهرت التدخلات العلاجية خلال الدراسة انخفاضًا ملحوظًا في مؤشرات الرفض، مما يفتح المجال لتطوير استراتيجيات علاجية موجهة تقلل من مخاطر رفض الأعضاء بشكل فعال.
التحديات العالمية في توافر الأعضاء وتحسين الحلول التقنية
- يعاني العالم من نقص شديد في الأعضاء البشرية المتاحة، مع تزايد أعداد المرضى المنتظرين ويزداد الوضع سوءًا باستمرار.
- وفي الولايات المتحدة، يتوفى أكثر من 13 شخصًا يوميًا أثناء انتظارهم لزراعة الأعضاء، بينما توفي مئات المرضى في دول أخرى بسبب نقص الأعضاء.
- رغم زيادة أعداد عمليات الزرع، فإن الطلب يفوق العرض بكثير، ويظل الحل الأكثر وعدًا هو الاعتماد على الأعضاء المعدلة وراثيًا من الخنازير.
الآفاق المستقبلية وتطوير العلاجات المناعية
مع استمرار الأبحاث، تتجه الأنظار نحو تحسين التعديلات الجينية للخنازير وتقليل احتمالات رفض الأعضاء. ويأمل العلماء أن تؤدي هذه التقنيات إلى جعل زراعة الأعضاء من الخنازير خيارًا واقعيًا ومستدامًا خلال عقد من الزمن، مما يساهم في إنقاذ آلاف الأرواح حول العالم.
وفي النهاية، فإن الوعي بأهمية هذه التطورات يوفر أملًا جديدًا لمرضى يحتاجون إلى زرع أعضاء، ويعزز من جهود الأبحاث المستمرة لتوفير حلول طويلة الأمد وفعالة لهذه المشكلة الصحية العالمية.