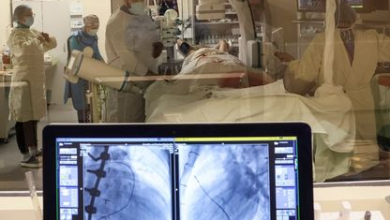
نجاح زراعة كلى الخنازير في البشر يصبح أقرب مما نتصور
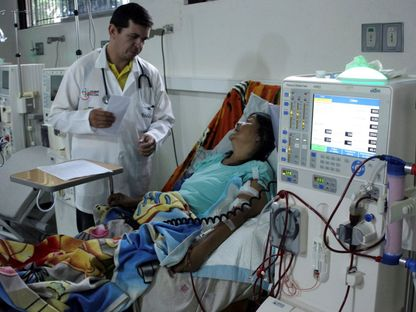
خرائط تفصيلية لتفاعل الخلايا المناعية مع أنسجة الكلى من الخنازير المزروعة للبشر
تمكن فريق من الباحثين من رسم خرائط متقدمة لكيفية تفاعل خلايا الجهاز المناعي البشرية مع أنسجة الكلى المستزرعة من الخنازير، باستخدام تقنيات تصوير جزيئي مكاني حديثة. يهدف هذا العمل إلى فهم أعمق لآليات الرفض المناعي وتحسين استراتيجيات العلاج للوصول إلى زرع أعضاء ناجح ومستدام.
تحديد الاستجابة المناعية المبكرة وتوقيت الرفض
- حدد الباحثون علامات جزيئية مبكرة تشير إلى حدوث الرفض المناعي، حيث ظهرت الأجسام المضادة في اليوم العاشر بعد الزرع وبلغت ذروتها في اليوم الثالث والثلاثين.
- أظهرت النتائج أن الرفض لا يبدأ بسرعة فحسب، بل يتطور عبر زمن معين، مما يوفر نافذة علاجية حاسمة للتدخل المبكر.
- استمرت الدراسة لمراقبة الاستجابات المناعية لمدة 61 يوماً، مما مكن الباحثين من تحديد «نافذة زمنية حرجة» للتدخل العلاجي بهدف تعزيز بقاء الأعضاء المزروعة.
آليات الرفض المناعي في زرع الأعضاء
يحدث الرفض عندما يتعرف الجهاز المناعي للمريض على العضو المزروع كـ«غريب»، ويدشن هجوماً تدميرياً بهدف القضاء عليه. وهناك آليتان رئيسيتان لهذا الرفض:
- الرفض الخلوي: وتحدثه الخلايا التائية التي تتعرف على المستضدات الغريبة وتهاجم الأنسجة.
- الرفض بوساطة الأجسام المضادة: حيث تتكون أجسام مضادة ضد مستضدات المتبرع، وتلتصق بالمَوضع، مما يؤدي إلى تنشيط الجهاز المناعي وتلف العضو.
التقدم في التجارب السريرية على زرع الخنازير المعدلة وراثياً
- بدأت التجارب السريرية في الولايات المتحدة في عام 2024، مع استخدام كلى خنزير معدلة وراثياً بعشرة تعديلات جينية، تشمل إضافة جينات بشرية وتعطيل جينات من الخنزير تقلل من احتمالية الرفض المناعي.
- حقق رجل يدعى ريتشارد سلايمان نجاحاً مؤقتاً، إذ استمرت الكلية المزروعة تؤدي وظيفتها بشكل جيد لمدة شهرين، رغم وفاته لاحقاً لسبب غير مرتبط بعملية الزرع.
- امرأة أخرى، تلقت كلية خنزير معدلة وراثياً لمدة 130 يوماً، قبل أن تتطلب إزالتها نتيجة لرفض حاد.
تفاعل الجهاز المناعي بين الإنسان والأعضاء المزروعة
توفر الدراسة خريطة دقيقة لتفاعل الخلايا المناعية، حيث تم تحديد أن خلايا الماكروفاج والخلايا النخاعية كانت الأكثر انتشاراً في عملية الرفض، وهو ما يؤكد دورها المركزي في استجابة الجهاز المناعي.
عند تطبيق تدخلات علاجية موجهة، لوحظ انخفاض ملحوظ في مؤشرات الرفض، مما يشير إلى إمكانية تعطيل التفاعل المناعي الضار وتقليل حالات رفض الأعضاء بشكل فعال.
التحديات العالمية ونقص الأعضاء
- يواجه العالم نقصاً حاداً في الأعضاء المتاحة للزرع، حيث يتجاوز الطلب العرض بكثير، مما يترك آلاف المرضى على قوائم الانتظار.
- على سبيل المثال، في الولايات المتحدة، ينتظر أكثر من 100 ألف مريض عملية زرع، وغالبية هؤلاء يحتاجون إلى كلى جديدة.
- رغم ارتفاع نشاط عمليات الزرع في عام 2024، لا تزال الحاجة تتجاوز الإمكانيات، مع وفاة العديد من المرضى أثناء انتظارهم، وتقدر التقديرات العالمية أن أقل من 10% من الطلب تلبيها عمليات الزرع الحالية.
آفاق تحسين العلاجات والزرع المستقبلي
تشير الدراسات إلى أن فهم التفاعل المناعي الجزيئي يضع الأسس لتطوير تدخلات مخصصة تمنع الرفض قبل حدوثه، وهو ما سيجعل زرع أعضاء الخنازير حلاً مستداماً ومسؤولاً عن أزمة النقص الحالية.
ويؤكد الخبراء أن الاعتماد الروتيني على هذه التقنية يتطلب سنوات من التجارب المستمرة، والتأكد من السلامة والفعالية، بالإضافة إلى الالتزام باللوائح التنظيمية، إلا أن نتائج الدراسات الحالية تقترب من جعل زراعة الكلى من الخنازير أكثر قرباً من الاستخدام الواسع.
وفي المستقبل، يركز الباحثون على تحسين العلاجات المناعية، وتعديل الخنازير وراثياً بشكل أدق، وتطوير بروتوكولات تنبيه مبكر لمراقبة علامات الرفض، بهدف جعل زراعة أعضاء الخنازير خياراً علاجياً مأموناً وفعالاً في السنوات المقبلة.